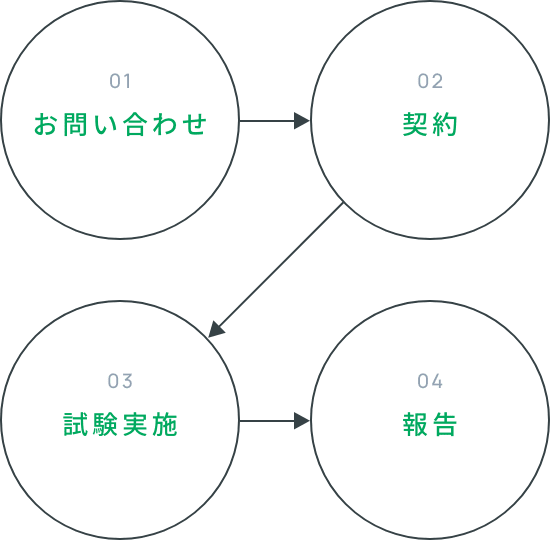
臨床試験の流れ

計画から試験実施、報告までトータルサポート
試験計画から倫理審査委員会(IRB)での審査、被験者募集、試験実施、データ集計、統計解析、報告まで行うことができるため、お客様のご要望に合わせた柔軟な対応が可能です。CPCCではトクホや機能性表示食品取得を目的とした参加者人数100名以上の規模の大きい臨床試験から、商品の効果を探索する10名前後のパイロット試験まで幅広く対応することができます。
01
お問い合わせ
お問い合わせから御見積
-

お問い合わせ
-

秘密保持契約締結
-

試験デザイン提案
-

御見積作成
臨床試験をお考えでしたら、まずはお問い合わせください。研究開発をしている製品情報を開示いただくこともありますので、必要であれば秘密保持契約を締結させていただきます。目的にあった最適な試験デザインの提案、ご予算に合わせて御見積を提示いたします。
02
契約
ご契約から倫理審査
-

試験委託
-

試験資料作成
-

倫理審査委員会
(IRB) -

試験許可
弊社にお任せいただける場合、委託書をいただき、施設スケジュールを確保し、倫理審査委員会(IRB)審査資料の作成を開始します。IRBで審査され、研究機関の長の許可を得た後、試験実施が可能になります。
03
試験実施
被験者募集から試験実施
-

被験者募集
-

事前検査
-

選定・割付
-

本試験
試験の条件に合った参加希望者を募集し、事前検査を実施します。
その中から試験に参加する被験者を選定、割付し、本試験へと進みます。
04
報告
データ集計から報告
-

データ集計
-

統計解析
-

報告書作成
-

論文/学会発表
試験で得られた検査結果やアンケート、日誌を集計します。試験が計画通り適切に実施されたか、集計に誤りがないか、記録が適切に保管されているか等モニタリングを行うこともあります。データ固定をして統計解析し、報告書にまとめます。ご要望に応じて論文作成、投稿まで対応いたします。

お問い合わせ
下記の内容を分かる範囲、開示できる範囲でお知らせください。対応可能か、ご連絡いたします。必要に応じて、電話、オンラインなどでお打ち合わせをさせていただきます。
- 試験の目的(社内データ、販売促進データ、論文投稿、機能性表示食品、トクホ など)
- 検証したい製品の情報(食品、飲料、サプリ、化粧品、機器 など)
- 評価したい内容(免疫機能、便通改善、肌のうるおい など)
- 摂取期間
- 試験人数
- 評価項目
- スケジュールの目安

秘密保持契約締結
貴社の重要な情報をご開示いただくにあたり、秘密保持契約を締結させていただくことがあります。

試験デザイン提案
WEB打ち合わせなどを通じてお客様の試験目的をヒアリングし、学術部門や専門家(医師、大学教授等)から得た、最新の知見情報に基づく最適な試験デザインをご提案いたします。

御見積作成
ヒアリングした内容で、試験費用を試算します。
ご予算に応じて、試験の一部のみを受託することも可能ですので、ご相談ください。

試験委託
施設のスケジュールを押さえるため、また被験者募集準備に、委託意思の提示として「委託書」をいただきます。
本契約は、倫理審査委員会承認後に締結させていただきます。(ご希望によっては、前になることもあります)

試験資料作成
倫理審査に必要な試験実施計画書、同意説明文書、同意書等の資料を作成します。

倫理審査委員会(IRB)
臨床試験が倫理性、安全性、科学的妥当性を満たし、倫理指針に基づき計画されているかを審査します。申請書類はIRB事務局で準備します。
基本的な審査資料:試験実施計画書、試験実施体制、試験品概要書、同意説明文書、同意書、同意撤回書(その他必要に応じて添付資料)

試験許可
倫理審査委員会の審査後、臨床試験を実施することが研究機関の長によって許可されます。原則的に、この段階で本契約を締結します。

被験者募集
弊社の被験者登録バンクから優先的に、不足する場合は外部の被験者募集機関から、条件に合った試験参加希望者を募集します。

事前検査
説明会を行い、参加者の試験参加同意取得の上、計画書で定められた検査項目を実施します。
試験の参加基準を満たしていない方や、遵守事項を守られていない方は、ご参加いただけません。

選定・割付
事前検査の検査結果などから参加者が適格性を満たしているか確認し、本試験に組み入れるかどうかを試験責任医師が総合的に判断します。選定された被験者を、割付責任者が割付因子を基に複数の群に分けます。適切に事前検査の記録が取られ、割付まで進んだかを確認するために、モニタリングを実施します。

本試験
計画書に従い実施します。被験者が遵守事項を守れているかどうか、WEB日誌などを通じて日々チェックします。有害事象があった場合は、速やかに状況の確認を行い、必要に応じて試験責任者の指示を仰ぎます。

データ集計
試験で得られた検査結果やアンケート、日誌等のデータを集計します。検査値や試験期間中の被験者の遵守事項の逸脱、有害事象の取り扱いなどを、症例検討会でお客様と協議し、データを固定します。データ固定後、割付情報を開示します(キーオープン)。

統計解析
経験豊富な学術スタッフがご希望を伺いながら統計解析計画をご提案し、キーオープン前までに統計解析計画書を作成します。
キーオープン後、予め取り決めた統計解析計画書に則り統計解析を行います。オプションとして、報告書提出後には、試験品の有効性への理解を深めるための探索的解析にも対応いたします。

報告書作成
試験結果を報告書に取りまとめて納品します。試験品の安全性・有効性について、医師・医学博士らによる臨床学的知見に加え、学術スタッフが統計学的観点から考察します。

論文/学会発表
ご依頼に応じて、報告書の論文化(和文/欧文)、学術誌への投稿、学会発表をサポートします。

